2024.06.14 - [배터리/지식] - 배터리의 작동 원리 및 소재-2(음극재)
배터리의 작동 원리 및 소재-2(음극재)
2024.06.12 - [배터리/지식] - 배터리의 작동 원리 및 소재-1(양극재) 배터리의 작동 원리 및 소재-1(양극재)2024.05.28 - [배터리/지식] - 배터리란 무엇인가? 이전 글에서는 배터리가 무엇인지, 종류는
dudqls3493.tistory.com
이전 글에서 배터리에 들어가는 음극재에 대해 살펴보았다.
음극재에 이어서 세번째로 알아볼 것은 전해질이다.
3. 배터리에 사용되는 소재
- 전해질(전해액)
사람은 대화를 할 때 공기의 진동을 통해 소리를 상대방에게 전달한다.
전해질은 배터리에서 양극재와 음극재 사이 Li+가 이동하기 위해 필요한 매질의 역할을 하는 소재이다.
쉽게 말해 이동수단인 것이다.
- 배터리 내의 전해질의 역할은 크게 2가지 이다.
① Li+의 이동 수단
② 양극재, 음극재 표면 보호
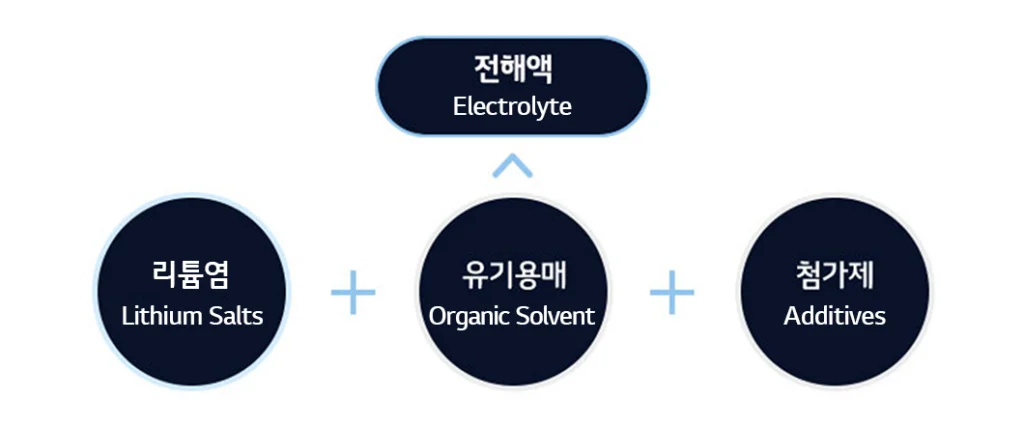
- 전해질은 총 3개의 요소가 합쳐져 있는 혼합물이다.

① 리튬염(Lithium-salt)
Li+가 이동하기 위해선 일종의 통로가 필요하다.
Li+는 통로 역할을 해주는 리튬염에 흡수가 되어 이동한다.
EV, 스마트폰, 테블릿PC등에 쓰이는 리튬염의 대부분은 LiPF6이 주로 사용된다고 한다.
그외 LiFSi(F전해질), LiPO2F2(P전해질), LiDFOP(D전해질), LiBOB(B전해질), LiBF4 등 소재들은
배터리의 요구 성능에 맞게 LiPF6과 함께 첨가 된다.
(기타 전해질 또한 LiPF6을 원재료로 파생된 소재들이며, 리튬염 제작 시 80~100%가 LiPF6이다.)
Q1. 왜 LiPF6이 주로 사용되는 걸까?
- 전해질이 가져야할 요구 조건을 LiPF6이 갖고 있고 다음과 같다.
① 적절한 용해도 높은 이온 전도성
② 우수한 전기화학적 안정성
③ 낮은 점도
④ 저온 및 고온에서의 온도 조건 최적화
LiPF6은 이미 배터리 전해질로서의 최적화 돼있는 소재로 알려져있고 실제로 사용되고 있다.
하지만 이러한 LiPF6에도 치명적인 단점이 존재한다.
바로 HF(황산가스)를 생성한다는 것이다.


배터리 내의 잔여 수분과 LiPF6과 반응을 하면 다음과 같이 LiPF6에 가수분해하여 반응식이 만들어진다.
LiPF6+H2O → HF(황산가스 발생) + PF5 + LiOH
여기서 HF가 발생하는데 양극활물질과 반응하여 금속이온이 용출이 된다.
- 이 금속이온은 왜 문제인가 하면 아래와 같은 다양한 문제를 야기하기 때문이다.
① 양극활물질의 구조적 붕괴로 인한 수명 및 에너지 밀도 감소
② 전해질 분해 가속화로 인한 전도성 감소
③ SEI(고체 전해질 계면층) 손상
④ 가스 발생으로 인한 배터리 폭발
⑤ 열적 불안정성
그렇다면 범용성은 뛰어나지만 여러가지 위험요소를 갖고 있는 LiPF6을 대체할 만한 소재가 있을까에 대한 의문점이 생긴다.
Q2. LiPF6을 대체할 소재로 LiFSi(F전해질)이 있다고 하는데..
1) LiPF6 vs LiFSi


Philippe, B., Dedryvère, R., Gorgoi, M., Rensmo, H., Gonbeau, D., & Edström, K. (2013).
Improved Performances of Nanosilicon Electrodes Using the Salt LiFSI: A Photoelectron Spectroscopy Study.
Journal of the American Chemical Society, 135(26), 9829-9842.
해당 논문의 내용에 따르면 LiPF6을 대체하여 LiFSi가 더 우수한 성능을 낸다는 연구결과가 있어서 참고했다.
LiFSI는 일반적인 LiPF6와 달리 장기적인 충전 주기 동안 실리콘 입자 표면의 플루오린화 과정을 방지한다고 한다.
(* 플루오린화 과정: 배터리 내 수분에 의해 HF와 같은 루이스 강산과 같은 플루오린화합물이 만들어지게 되는 것)
그 결과 표면 실리콘 상의 조성이 변화하고 바인더와 활성 물질 표면 간의 유리한 상호작용이 유지된다고 한다.
2) LiPF6 vs LiFSi의 충방전 시 전기화학 성능 비교

- (a), (b) 150mA/g 및 700mA/g 에서의 방전 사이클 비교
사이클이 진행될수록 용량 감소가 발생하지만, LiFSi의 경우 LiPF6 대비 용량 감소가 훨씬 작은 것을 알 수 있다.
120 사이클 후, LiPF6는 약 300 mAh/g의 용량을 유지하는 반면, LiFSI는 약 1300 mAh/g의 용량을 유지한다.
- (c) 서로 다른 전류 속도에서의 방전 용량 대 사이클 수 (C/10 ~10C)
모든 전류량에서 LiFSi는 LiPF6보다 더 나은 방전 능력을 보여주고 있다.
즉, 사이클이 지속됨에 따라 방전 용량이 LiFSi가 상대적으로 더 적다는 것을 보여주고 있다.
- (d) 고정 용량 테스트 (방전 용량 1200 mAh/g로 제한)
동일 방전 용량에서 LiPF6는 46 사이클을 유지하지만 LiFSI는 147 사이클 동안 유지하는 것을 확인할 수 있다.
3) 결론
논문에 의하면 LiFSi가 LiPF6보다 실리콘 전극의 전기화학적 성능을 크게 향상시키는 결과를 보여줬다.
이는 주로 LiFSi의 낮은 가수분해 민감성과 안정적인 SEI층 형성에 의함이라고 한다.
이로 인해 LiFSi는 장기 사이클링 동안 더 우수한 용량 유지와 전극 안정성을 제공한다는 결론이다.
② 유기 용매(Organic Solvent)
유기 용매는 Li+가 리튬염에 잘 용해될 수 있도록 서브해주는 역할을 한다.
유기 용매로서 사용되기 위해선 몇가지 조건을 갖춰야 한다.
1) 유기용매 조건 및 종류

- 유기 용매의 조건
① 유전율이 높아야 한다 *유전율(Permittivity): 이온 화합물 분리 능력
② Li+ 이동을 위한 낮은 점도
Li+의 원활한 이동을 위해선 이온화도와 이온 전도성이 높아야 한다.
그렇기 이온 화합물 분리 능력의 척도인 유전율과 자체 점도가 낮야아 한다.
- 유기 용매의 조건
① 유전율이 높아야 한다 *유전율(Permittivity): 이온 화합물 분리 능력
② Li+ 이동을 위한 낮은 점도
- 유기 용매의 종류
앞서 언급했듯 유전율이 높고 점도가 낮은 용매가 적절한 용매이다.
유기 용매는 기본용매와 보조용매의 혼합물로 다음과 같이 사용된다.
기본용매: 고리형 카보네이트(EC,PC) + 보조용매: 사슬형 카보네이트(DMC,EMC,DEC)
③ 첨가제(Additives)
첨가제는 전해액의 성능 개선을 위해 약 5%정도의 소량 첨가되는 물질이지만 중요한 역할을 하고있다.
- 첨가제를 사용하는 구체적인 이유는 다음과 같다.
① 성능 향상: 전해질의 이온 전도성을 높이고, 저온 및 고온 환경에서의 배터리 성능을 유지한다.
② 안정성 제공: SEI 층의 형성과 안정화를 통해 전극의 부식과 분해를 방지한다.
③ 수명 연장: 과충전 및 과방전 보호, 전해질 분해 억제를 통해 배터리의 수명을 증가시킨다.
④ 안전성 개선: 가스 발생 억제, 전극 부식 방지를 통해 배터리의 안전성을 높인다.
- 첨가제들의 종류는 다음과 같다.
① SEI층 형성 첨가제
- 비닐렌 카보네이트(VC): SEI 층의 안정성을 높이고, 전극 표면의 부식과 분해를 억제함.
- 플루오로에틸렌 카보네이트(FEC): SEI 층의 전기화학적 안정성을 향상시킴.
② 고온 안정성 첨가제
- 이온성 액체(Ionic Liquids): 높은 열 안정성을 제공하여 고온 환경에서도 전해질의 성능을 유지할 수 있음.
- 알킬 카보네이트: 고온에서의 전해질 분해를 억제하여 배터리의 안전성을 향상시킴.
③ 저온 성능 개선 첨가제
- 설폰산 에스터: 저온 환경에서 전해질의 점도를 낮춰 이온 이동을 원활하게 하여 배터리 성능을 향상시킴.
- 에틸렌 카보네이트(EC): 저온에서의 전해질 전도성을 유지할 수 있음.
④ 과충전 및 과방전 보호 첨가제
- 리튬 비스(옥살라토)보레이트(LiBOB): 과충전 및 과방전 시 전극의 안정성을 높여 배터리 수명을 연장시킴.
- 붕산 에스터(Borate Esters): 과충전 방지를 위해 사용됨.
⑤ 전해질 안정화 첨가제
- 인산 에스터(Phosphate Esters): 전해질의 산화 안정성을 높여 고전압 전지의 성능을 개선시킴.
- 트리메틸 포스페이트(TMP): 전해질의 안정성을 높여 고전압 조건에서의 분해를 억제함.
⑥ 전도성 향상 첨가제
- 리튬 테트라플루오로보레이트(LiBF4): 전해질의 이온 전도성을 향상시켜 배터리 성능 향상시킴.
- 리튬 플루오로설폰이미드(LiFSI): 높은 전도성 제공 (앞서 설명했던 LiPF6 대체재로서 활용되는 소재)
⑦ 부식 방지 첨가제
- 트리플루오로메탄설폰이미드(TFSI): 알루미늄 호일 등의 전극 부식을 방지하여 전지의 수명을 연장시킴.
- 리튬 불화 포스페이트(LiPF6): 알루미늄 부식을 억제하는 데 사용됨.
⑧ 가스 발생 억제 첨가제
- 다이페닐 카보네이트(DPC): 충전 및 방전 과정에서 발생하는 가스를 억제하여 배터리 내부 압력을 저하시킴.
- 티오글리콜레이트(TGA): 전극 반응 시 가스 발생을 줄여 배터리의 안정성을 향상 시킴.
* 최근 장거리 주행 실현 가능한 배터리 첨가제 기술 개발

Smith, J.; Doe, A.; Brown, B.
Elastic Interfacial Layer Enabled the High-Temperature Performance of Lithium-Ion Batteries
via Utilization of Synthetic Fluorosulfate Additive.
*Journal of the American Chemical Society* 2023, *145*(12), 5678-5690.
최근 KAIST-고려대-UNIST-현대자동차-KRICT에서 전해질 첨가제 APFS를 개발했다고 한다.
충방전을 반복할 수록 용량 감소, 양극재 구조 붕괴 및 음극재의 스웰링 현상이 성능과 안정성에 문제를 야기하게 된다.
이로 인해 전해질은 Li+ 이동 뿐만아니라 위와 같은 문제들을 해결하기 위한 필수적인 요소이다.
이를 위해 SEI층 활성화가 중요한데 해당 기능을 하는 첨가제로 VC,FEC가 있다.
APFS는 기존 VC,FEC 대비 54%, 38% 성능 향상을 보여주었다.
이번 글에서는 전해액에 대해서 알아보았다.
양극재와 음극재를 연결해주는 전해액은 중요한 소재이다.
다음글에서는 분리막을 마지막으로 소개하고자 한다.
감사합니다 :)
'배터리 > 지식' 카테고리의 다른 글
| 배터리의 작동 원리 (1) | 2024.07.01 |
|---|---|
| 배터리의 작동 원리 및 소재-4(분리막) (0) | 2024.06.21 |
| 배터리의 작동 원리 및 소재-2(음극재) (1) | 2024.06.14 |
| 배터리의 작동 원리 및 소재-1(양극재) (0) | 2024.06.12 |
| 배터리란 무엇인가? (2) | 2024.05.28 |



